Il recente outbreak di malattia da Coronavirus 2019 (COVID-19), causata dal Severe acute respiratory syndrome coronavirus-2 (SARS-CoV-2) è esitato in una pandemia mondiale. Sebbene la malattia polmonare disseminata, con lo sviluppo di Acute respiratory distress syndrome (ARDS), rappresenti la principale causa di morbidità e mortalità nel COVID-19, il coinvolgimento epatico appare significativo, da una parte correlato alla severità di malattia, dall’altra sembra fungere da fattore prognostico per lo sviluppo di complicanze nell’ARDS. Lo spettro di danno epatico nel COVID-19 può spaziare dall’infezione diretta da parte di SARS-CoV-2, al coinvolgimento indiretto da infiammazione sistemica, ai danni ipossici, a cause iatrogene (farmaci) e comportare l’esacerbazione di una epatopatia preesistente. Questa breve revisione presenta i possibili meccanismi fisiopatologici del tropismo epatico di SARS-CoV-2 e le alterazioni epatiche acute e croniche in corso di COVID-19.
I meccanismi di danno epatico da SARS-CoV-2
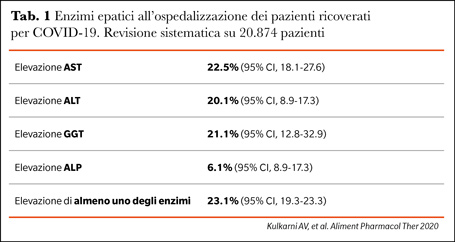 Una revisione sistematica su 20.874 pazienti ricoverati per COVID-19 ha documentato che nel 23% dei casi vi era un incremento di almeno uno degli enzimi epatici (transaminasi, gamma-gt o fosfatasi alcalina) all’ospedalizzazione (Tabella 1), e che vi era una più elevata probabilità di presentare transaminasi elevate all’ingresso nei pazienti più gravi o che andavano incontro a morte, rispetto a quelli con presentazione meno severa e che sopravvivevano (OR 2.87 e 3.46, rispettivamente) (1). Nei pazienti con enzimi epatici normali all’ospedalizzazione vi era una probabilità del 50% di un successivo incremento degli enzimi epatici durante il ricovero, con percentuali significativamente maggiori nei trattati con lopinavir/ritonavir (2).
Una revisione sistematica su 20.874 pazienti ricoverati per COVID-19 ha documentato che nel 23% dei casi vi era un incremento di almeno uno degli enzimi epatici (transaminasi, gamma-gt o fosfatasi alcalina) all’ospedalizzazione (Tabella 1), e che vi era una più elevata probabilità di presentare transaminasi elevate all’ingresso nei pazienti più gravi o che andavano incontro a morte, rispetto a quelli con presentazione meno severa e che sopravvivevano (OR 2.87 e 3.46, rispettivamente) (1). Nei pazienti con enzimi epatici normali all’ospedalizzazione vi era una probabilità del 50% di un successivo incremento degli enzimi epatici durante il ricovero, con percentuali significativamente maggiori nei trattati con lopinavir/ritonavir (2).
I meccanismi fisiopatologici e immunologici di danno epatico nei pazienti con COVID-19 non sono del tutto chiariti ma comprendono: un effetto citopatico diretto del virus, un’anomala risposta immunitaria, l’alterazione della coagulazione ed il danno da ischemia/ipossia e riperfusione. ACE2, il recettore suscettibile per l'ingresso di SARS-CoV-2 nelle cellule, è presente nelle cellule alveolari di tipo 2, nel tratto gastroenterico e nel fegato ed è altamente espresso nello strato endoteliale dei piccoli vasi sanguigni, ma non nell'endotelio sinusoidale. ACE2 è inoltre maggiormente espresso nei colangiociti (59%) rispetto agli epatociti (3%), in concentrazioni simili a quelle delle cellule alveolari di tipo 2 dei polmoni, indicando come il fegato sia un potenziale bersaglio del virus.
SARS-CoV-2 determina di per sé un danno diretto agli epatociti provocando il rigonfiamento dei mitocondri, la dilatazione del reticolo endoplasmatico, la riduzione dei granuli di glicogeno e la compromissione delle membrane cellulari. L’anomala risposta immunitaria dell’organismo al virus è caratterizzata da tre fasi:
- attivazione immunitaria
- linfoistiocitosi emofagocitaria secondaria (una sindrome iperinfiammatoria caratterizzata da cellule T attivate e cellule NK che producono grandi quantità di citochine che attivano macrofagi derivati da monociti) e
- soppressione immunitaria (3).
Nella fase di attivazione immunitaria, la replicazione di SARS-CoV-2 provoca un particolare tipo di morte cellulare chiamato piroptosi con rilascio di citochine pro-infiammatorie che a loro volta attivano le cellule T e B e reclutano macrofagi e monociti (4). I macrofagi attivati producono ulteriore IL-6 e altri fattori infiammatori, con conseguente rilascio di citochine, determinando la cosiddetta tempesta di citochine che provoca gravi danni immunitari ai polmoni e al fegato, a cui fa seguito la fase della soppressione immunitaria caratterizzata da una drastica riduzione dei linfociti periferici, apoptosi ed esaurimento delle cellule T (5). In risposta agli stimoli pro-infiammatori vi è un’attivazione piastrinica e della coagulazione con un danno endoteliale, e proprio l’alterazione della coagulazione è stata associata alla prognosi più sfavorevole nei pazienti con COVID-19 e grave disfunzione epatica.
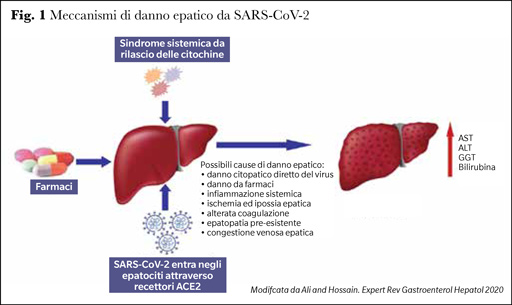 Infine, vi è il danno epatico da ischemia/ipossia riperfusione, caratterizzato da una fase di danno cellulare da ischemia e successiva risposta infiammatoria indotta dalla riperfusione, che determina apoptosi degli epatociti e conseguente aumento degli enzimi epatici (6). Nei pazienti con COVID-19 vi può essere anche un danno epatico indotto dai farmaci (antibiotici, antivirali e immunosoppressori soprattutto), i cui meccanismi sono variabili e includono risposte immunitarie sregolate con livelli plasmatici di citochine pro-infiammatorie (IL-6 e TNF-α) marcatamente elevate e danno citopatico (Figura 1) (7). Uno studio su 48 pazienti deceduti per COVID-19 ha documentato a livello istologico una marcata alterazione della rete dei vasi sanguigni intraepatici secondaria ai cambiamenti sistemici indotti dal virus pur senza un danno infiammatorio epatico significativo (8).
Infine, vi è il danno epatico da ischemia/ipossia riperfusione, caratterizzato da una fase di danno cellulare da ischemia e successiva risposta infiammatoria indotta dalla riperfusione, che determina apoptosi degli epatociti e conseguente aumento degli enzimi epatici (6). Nei pazienti con COVID-19 vi può essere anche un danno epatico indotto dai farmaci (antibiotici, antivirali e immunosoppressori soprattutto), i cui meccanismi sono variabili e includono risposte immunitarie sregolate con livelli plasmatici di citochine pro-infiammatorie (IL-6 e TNF-α) marcatamente elevate e danno citopatico (Figura 1) (7). Uno studio su 48 pazienti deceduti per COVID-19 ha documentato a livello istologico una marcata alterazione della rete dei vasi sanguigni intraepatici secondaria ai cambiamenti sistemici indotti dal virus pur senza un danno infiammatorio epatico significativo (8).
COVID-19 e malattia epatica cronica
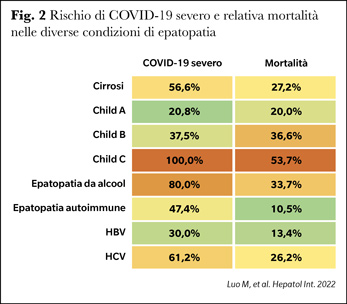 I pazienti con malattia cronica di fegato sono poco rappresentati nelle coorti di pazienti con COVID-19, costituendo meno dell'1% dei casi (9). I danni epatici da SARS-CoV-2 sono solitamente lievi e autolimitanti, mentre le forme più avanzate correlano con un decorso clinico più grave con tassi più elevati di ricovero in terapia intensiva, ventilazione meccanica, dialisi e mortalità (10), ed è descritto un rischio più elevato di scompenso ed insufficienza epatica nei pazienti con riserva funzionale epatica maggiormente compromessa. Le anomalie dei test di funzionalità epatica variano dal 37% al 69%, raggiungendo l'80% nei pazienti successivamente deceduti. Livelli di transaminasi superiori a 5 volte la norma si sono associati ad un aumentato rischio di morte (11). Uno dei più grandi studi americani su pazienti con epatopatia cronica ha documentato come l’infezione da SARS-CoV-2 nei cirrotici fosse associata ad un rischio di morte 2.38 volte superiore rispetto ai non infetti ma, soprattutto, come la cirrosi fosse associata ad un rischio di morte 3.31 volte superiore rispetto ai non cirrotici (12), confermando i tassi di mortalità del 30% precedentemente segnalati nei cirrotici in Italia (13). In Figura 2 sono riportati i tassi di COVID-19 severo (necessità di ricovero, ricovero in terapia intensiva o di ventilazione) e di mortalità complessiva per le diverse eziologie e le diverse classi di Child-Pugh (14).
I pazienti con malattia cronica di fegato sono poco rappresentati nelle coorti di pazienti con COVID-19, costituendo meno dell'1% dei casi (9). I danni epatici da SARS-CoV-2 sono solitamente lievi e autolimitanti, mentre le forme più avanzate correlano con un decorso clinico più grave con tassi più elevati di ricovero in terapia intensiva, ventilazione meccanica, dialisi e mortalità (10), ed è descritto un rischio più elevato di scompenso ed insufficienza epatica nei pazienti con riserva funzionale epatica maggiormente compromessa. Le anomalie dei test di funzionalità epatica variano dal 37% al 69%, raggiungendo l'80% nei pazienti successivamente deceduti. Livelli di transaminasi superiori a 5 volte la norma si sono associati ad un aumentato rischio di morte (11). Uno dei più grandi studi americani su pazienti con epatopatia cronica ha documentato come l’infezione da SARS-CoV-2 nei cirrotici fosse associata ad un rischio di morte 2.38 volte superiore rispetto ai non infetti ma, soprattutto, come la cirrosi fosse associata ad un rischio di morte 3.31 volte superiore rispetto ai non cirrotici (12), confermando i tassi di mortalità del 30% precedentemente segnalati nei cirrotici in Italia (13). In Figura 2 sono riportati i tassi di COVID-19 severo (necessità di ricovero, ricovero in terapia intensiva o di ventilazione) e di mortalità complessiva per le diverse eziologie e le diverse classi di Child-Pugh (14).
Al contrario, i pazienti con epatopatie autoimmuni che contraggono il virus non hanno una prognosi peggiore. Durante il picco epidemico di inizio 2020 nel Nord Italia, in 148 pazienti con epatopatie autoimmuni sono stati registrati solo 4 casi confermati di COVID-19 ed un solo decesso (15). In uno studio internazionale che ha coinvolto 70 pazienti epatopatici non è stata osservata alcuna differenza nelle ospedalizzazioni, nei ricoveri in terapia intensiva e nella mortalità in chi aveva autoimmunità rispetto a chi non l’aveva (16). Ed infine, un ulteriore studio italiano che ha valutato il decorso clinico di 10 pazienti con epatite autoimmune in trattamento immunosoppressivo e COVID-19, ha riportato un solo decesso per scompenso della cirrosi, in una paziente che aveva sospeso i corticosteroidi all’esordio di infezione (17). L'esperienza finora accumulata suggerisce pertanto che i pazienti, sia pediatrici che adulti, in terapia immunosoppressiva per epatopatie autoimmuni non siano più vulnerabili all'infezione da SARS-CoV-2 rispetto alla popolazione generale e ciò supporta l'idea che il trattamento immunosoppressivo non debba essere modificato o interrotto in questi soggetti senza COVID-19.
Un dato rilevante che è emerso indica come l’obesità, il diabete e l’ipertensione arteriosa siano fattori di rischio per un decorso più severo di COVID-19. Recentemente si è dimostrato come l'ACE2 sia sovra-regolato nei tessuti adiposi sottocutanei e viscerali e nel tessuto epatico di individui con malattia da fegato grasso, favorendo la penetrazione virale in associazione alla già nota capacità del tessuto adiposo di fungere da amplificatore della risposta infiammatoria. Per tale ragione la MAFLD (Metabolic dysfunction-associated fatty liver disease) si associa ad una prognosi più severa da COVID-19, anche in pazienti giovani e non diabetici (18). Hu e colleghi hanno riportato in uno studio di 58 pazienti infettati da SARS-CoV-2 con sovrappeso/obesità e alterata funzionalità epatica, come proprio l'obesità sia un fattore predisponente un più prolungato ricovero (19). In una coorte retrospettiva di 202 pazienti con COVID-19 e NAFLD (Non-alcoholic fatty liver disease), un’alterazione degli enzimi epatici è stata osservata nel 50% e 75% dei pazienti all’ospedalizzazione e durante il ricovero, rispettivamente. La maggior parte dei pazienti con danno epatico persistente aveva NAFLD e BMI elevato ed i pazienti con NAFLD presentavano anche un rischio più elevato di progressione a manifestazione più grave di COVID-19 (20). Anche nei pazienti con MAFLD si è confermato come la gravità delle manifestazioni da COVID-19 sia notevolmente aumentata nei pazienti con score non invasivi per la fibrosi (FIB-4) più elevati, indipendentemente dalle co-morbidità metaboliche, a dimostrare proprio come la presenza della MAFLD con fibrosi significativa/avanzata possa esacerbare la tempesta di citochine indotta dal virus, probabilmente attraverso il rilascio epatico di più citochine pro-infiammatorie (21).
Take-home messages
- In corso di infezione da SARS-CoV-2 è frequente l’elevazione degli enzimi epatici che si associano in genere con una malattia più severa caratterizzata da più elevata mortalità.
- L’elevazione degli enzimi epatici è un epifenomeno dell’infiammazione sistemica e dell’alterazione dei processi coagulativi. Al danno epatico contribuiscono anche l’ipossia, la congestione epatica e, potenzialmente, le terapie farmacologiche utilizzate per il trattamento del COVID-19.
- Le malattie epatiche autoimmuni non presentano un rischio addizionale in caso di COVID-19 e i regimi immunosoppressivi in corso non dovrebbero essere modificati.
- Tra le epatopatie non cirrogene la MAFLD è quella a maggior rischio per lo sviluppo di una forma severa di COVID-19.
- I pazienti cirrotici sono quelli a maggior rischio di severità e mortalità da COVID-19 e la compromissione della funzione epatica è predittiva di eventi avversi. I cirrotici ospedalizzati per COVID-19 vanno incontro al decesso più comunemente per complicanze respiratorie che per scompenso dell’epatopatia.
- Kulkarni AV, Kumar P, Tevethia HV, et al. Systematic review with meta-analysis: liver manifestations and outcomes in COVID-19. Aliment Pharmacol Ther 2020;52:584-599.
- Fan Z, Chen L, Li J, et al. Clinical features of COVID-19-related liver functional abnormality. Clin Gastroenterol Hepatol 2020;18:1561-1566.
- Li D, Ding X, Xie M, et al. COVID-19-associated liver injury: from bedside to bench. J Gastroenterol 2021;56:218-230.
- Feng G, Zheng KI, Yan QQ, et al. COVID-19 and liver dysfunction: current insights and emergent therapeutic strategies. J Clin Transl Hepatol 2020;8:18-24.
- Mehta P, McAuley DF, Brown M, et al. COVID-19: consider cytokine storm syndromes and immunosuppression. Lancet 2020;395:1033-1034.
- Peralta C, Jimenez-Castro MB, Gracia-Sancho J. Hepatic ischemia and reperfusion injury: effects on the liver sinusoidal milieu. J Hepatol 2013;59:1094-1106.
- Ali N, Hossain K. Liver injury in severe COVID-19 infection: current insights and challenges. Expert Rev Gastroenterol Hepatol 2020;14:879-884.
- Sonzogni A, Previtali G, Seghezzi M, et al. Liver histopathology in severe COVID 19 respiratory failure is suggestive of vascular alterations. Liver Int 2020;40:2110-2116.
- Williamson E, Walker AJ, Bhaskaran KJ, et al. Open SAFELY: factors associated with COVID-19-related death using openSAFELY. Nature2020;584:430-436.
- Piano S, Dalbeni A, Vettore E, et al. Abnormal liver function tests predict transfer to intensive care unit and death in COVID-19. Liver Int 2020;40:2394-2406.
- Cai Q, Huang D, Yu H, et al. COVID-19: abnormal liver function tests. J Hepatol 2020;73:566-574.
- Ge J, Pletcher MJ, Lai J, et al. Outcomes of SARS-CoV-2 infection in patients with chronic liver disease and cirrhosis: a national COVID cohort collaborative study. Gastroenterology 2021;161:1487-1501.
- Iavarone M, D’Ambrosio R, Soria A, et al. High rates of 30-day mortality in patients with cirrhosis and COVID-19. J Hepatol 2020;73:1063-1071.
- Luo M, Ballester MP, Soffientini U, et al. SARS-CoV-2 infection and liver involvement.Hepatol Int. 2022;16:755-774.
- Di Giorgio A, Nicastro E, Speziani C, et al. Health status of patients with autoimmune liver disease during SARS-CoV-2 outbreak in northern Italy. J Hepatol 2020;73:702-705.
- Marjot T, Buescher G, Sebode M, et al. SARSCoV-2 infection in patients with autoimmune hepatitis. J Hepatol 2021;74:1335-1343
- Gerussi A, Rigamonti C, Elia C, et al. Coronavirus Disease 2019 in autoimmune hepatitis: a lesson from immunosuppressed patients. Hepatol Commun 2020;4:1257-1262.
- Ryan PM, Caplice NM. Is adipose tissue a reservoir for viral spread, immune activation, and cytokine amplifcation in coronavirus disease 2019? Obesity 2020;28:1191-1194.
- Hu X, Pan X, Zhou W, et al. Clinical epidemiological analyses of overweight/obesity and abnormal liver function contributing to prolonged hospitalization in patients infected with COVID-19. Int J Obes 2020;44:1784-1789.
- Ji D, Qin E, Xu J, et al. Non-alcoholic fatty liver diseases in patients with COVID-19: a retrospective study. J Hepatol 2020;73:451-453.
- Targher G, Mantovani A, Byrne CD, et al. Risk of severe illness from COVID-19 in patients with metabolic dysfunction-associated fatty liver disease and increased fibrosis scores. Gut 2020;69:1545-1547.






