I donatori anti-HCV positivi rappresentano una preziosa risorsa nel tentativo di colmare il divario tra necessità terapeutica di trapianto e disponibilità di organi.
I dati disponibili in letteratura sui donatori di fegato HCV positivi, per lo più pubblicati in epoca interferonica, non hanno dimostrato un impatto di tali donatori sulla sopravvivenza di organo e di paziente, impiegando organi con una fibrosi massima di 2/6 secondo Ishak (1). In particolare, è stato recentemente pubblicato un lavoro americano su 33.668 riceventi HCV positivi trapiantati di fegato tra il 1995 ed il 2013; il 5,7% ha ricevuto un organo HCV positivo e, confrontato con i riceventi di organi HCV negativi, non ha dimostrato una differenza statisticamente significativa sino a 10 anni di follow-up, in termini di sopravvivenza (2).
Lo studio di Lai e coll. (3) del 2012 su 1206 riceventi HCV positivi, di cui l’8% trapiantato con un organo HCV positivo, ha dimostrato un impatto dell’età del donatore (se superiore a 45 anni) sulla progressione della fibrosi del graft. Occorre tuttavia tener presente che in epoca interferonica la terapia antivirale veniva introdotta a fronte di una recidiva epatitica post-trapianto con almeno una fibrosi moderata (≥ 2).
A partire da agosto 2015, in USA (UNOS policy) è stato introdotto l’obbligo di testare, al momento della donazione, i donatori HCV positivi per l’HCV RNA, suddividendo pertanto i donatori HCV positivi in viremici (con infezione attiva) e non viremici (considerati a bassissimo rischio di trasmettere infezione) (4).
Degno di nota, uno studio presentato all’AASLD del 2017 su 25 pazienti HCV negativi che hanno ricevuto un fegato HCV anticorpi-positivo, HCV RNA NAT negativo: ha mostrato un 16% di positivizzazione del virus post-trapianto entro 11 mesi di mediana (5). I donatori di tali riceventi erano di età inferiore ai 40 anni, tutti morti di overdose. Nel 2010, in USA, la percentuale di fegati HCV positivi allocati a riceventi HCV positivi è stata del 7%, nel 2015 del 17% e, sempre nel 2015, la percentuale di fegati HCV positivi scartati rispetto a quelli HCV negativi si è ridotta da 3 volte (prima del 2010) a 1.7 volte (6).
Il recente incremento in USA delle morti giovanili per overdose e l’avvento degli antivirali ad azione diretta (DAA) spiegano l’aumento nell’uso di donatori HCV positivi.
I DAA, in considerazione della loro straordinaria efficacia e ottima tollerabilità, hanno infatti rappresentato una vera rivoluzione per l’epatite HCV, in particolare in ambito trapiantologico. Possono infatti essere impiegati più o meno precocemente post-trapianto, consentendo la guarigione dall’infezione in oltre il 95% dei pazienti trattati (7). Nel caso di donatore HCV viremico, l’impiego di DAA pangenotipici consente di bypassare il problema della coesistenza/dominanza genotipica tra donatore e ricevente.
Ad oggi esistono ancora pochissimi dati sull’impiego di donatori HCV positivi in epoca DAA. L’esperienza torinese tra il 2014 e il 2016 su 83 riceventi HCV positivi, di cui 11 trapiantati con organi HCV positivi (7/11 viremici), ha dimostrato, seppur su piccoli numeri, un outcome assolutamente confrontabile in termini di sopravvivenza, rigetto, early allograft dysfunction e complicanze biliari rispetto ai riceventi di organi HCV negativi (8).
Il numero di riceventi HCV viremici in attesa di trapianto, in considerazione della progressiva larga diffusione dei DAA, si sta riducendo e sono stati pubblicati sinora alcuni case report/piccole casistiche sull’impiego di donatori HCV viremici di fegato, rene, cuore e polmone in riceventi HCV negativi (Tabella 1). I risultati, ancorché su piccoli numeri, sono incoraggianti e di stimolo a trial multicentrici.
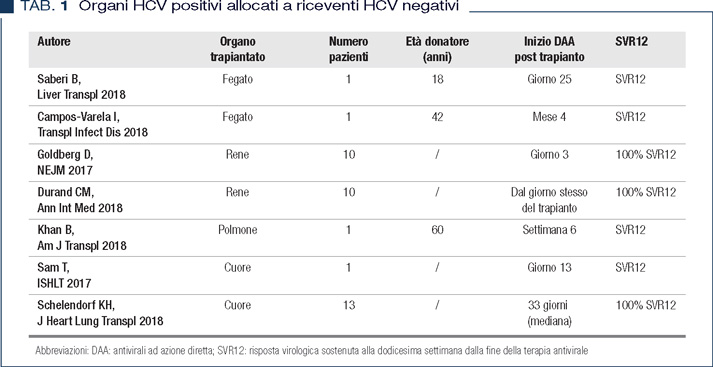
Si rendono peraltro necessari anche trial atti a valutare il grado massimo di fibrosi accettabile nel caso di donatori di fegato HCV positivi.
Recentemente è stato pubblicato un caso di un paziente sottoposto a trapianto di fegato a Torino con un organo HCV positivo e fibrosi 3/6 secondo Ishak (9). Il paziente ha raggiunto la risposta virologica sostenuta a 48 settimane dalla fine delle 24 settimane di DAA e la biopsia epatica più l’elastografia epatica a 72 settimane post-trapianto hanno evidenziato una regressione della fibrosi ad 1/6 secondo Ishak (10).
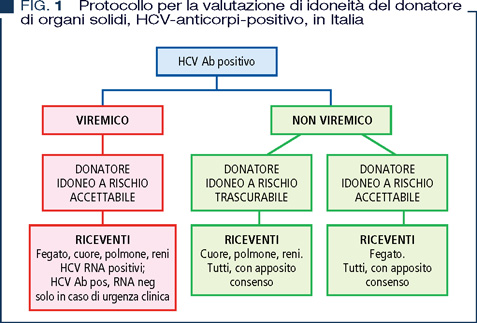 In Italia il protocollo per la valutazione di idoneità del donatore di organi solidi con positività per anticorpi anti-epatite C, prevede la valutazione dell’HCV RNA al momento della donazione al fine di distinguere i viremici dai non viremici. Il donatore viremico viene considerato idoneo, a rischio accettabile, ed allocato a riceventi di fegato/cuore/polmone/reni HCV RNA positivi; viene allocato a riceventi non viremici esclusivamente in caso di urgenza clinica. Il donatore HCV non viremico viene considerato idoneo, a rischio trascurabile, ed allocato a riceventi di cuore/polmone/reni; nella donazione di fegato (essendo quest’ul-timo il principale eventuale reservoir del virus), l’organo viene considerato idoneo, a rischio accettabile, ed allocato a qualunque paziente in attesa di trapianto di fegato (Figura 1), previa opportuna acquisizione di consenso informato.
In Italia il protocollo per la valutazione di idoneità del donatore di organi solidi con positività per anticorpi anti-epatite C, prevede la valutazione dell’HCV RNA al momento della donazione al fine di distinguere i viremici dai non viremici. Il donatore viremico viene considerato idoneo, a rischio accettabile, ed allocato a riceventi di fegato/cuore/polmone/reni HCV RNA positivi; viene allocato a riceventi non viremici esclusivamente in caso di urgenza clinica. Il donatore HCV non viremico viene considerato idoneo, a rischio trascurabile, ed allocato a riceventi di cuore/polmone/reni; nella donazione di fegato (essendo quest’ul-timo il principale eventuale reservoir del virus), l’organo viene considerato idoneo, a rischio accettabile, ed allocato a qualunque paziente in attesa di trapianto di fegato (Figura 1), previa opportuna acquisizione di consenso informato.
In conclusione, il tasso di utilizzo dei donatori HCV positivi è in progressivo aumento grazie soprattutto all’avvento degli antivirali ad azione diretta che consentono di guarire l’infezione in una elevata percentuale di pazienti. Si rimane in attesa di dati solidi in merito alla allocazione di tali organi anche in pazienti HCV negativi.
Bibliografia
- Coilly A, Samuel D. Pros and Cons: Usage of organs from donors infected with hepatitis C virus - Revision in the direct-acting antiviral era. J Hepatol 2016; 64:226-31.
- Stepanova M, Sayiner M, de Avila L, et al. Long-term outcomes of liver transplantation in patients with hepatitis C infection are not affected by HCV positivity of a donor. BMC Gastroenterol. 2016; 16:137-42.
- Lai JC, O’Leary JG, Trotter JF, et al. Risk of advanced fibrosis with grafts from hepatitis C antibody-positive donors: a multicenter cohort study. Liver Transpl 2012; 18:532-8.
- Levitsky J, Formica RN, Bloom RD, et al. The American Society of Transplantation Consensus Conference on the Use of Hepatitis C Viremic Donors in Solid Organ Transplantation. Am J Transplant. 2017; 17:2790-802.
- Bari K, Luckett K, Kaiser T, et al. Hepatitis C transmission from seropositive, nonviremic donors to non-hepatitis C liver transplant recipients. Hepatology 2018; 67:1673-82.
- Bowring MG, Kucirka LM, Massie AB, et al. Changes in Utilization and Discard of Hepatitis C-Infected Donor Livers in the Recent Era. Am J Transplant. 2017; 17:519-27.
- EASL Recommendations on Treatment of Hepatitis C 2018. J Hepatol 2018, in press. www.easl.eu.
- Martini S, Tandoi F, Pittaluga F, et al. Optimizing Allocation of Grafts From Hepatitis C Virus Antibody-Positive Donors Through Urgent Serum HCV RNA Determination. Hepatology 2018 (suppl 1);1A.
- Martini S, David E, Tandoi F, et al. HCV viremic donors with hepatic bridging fibrosis: Are we ready to use their livers in the era of direct-acting antivirals? Am J Transplant. 2017; 17:2986-7.
- Centro Nazionale Trapianti. Protocollo per la valutazione di idoneità del donatore di organi solidi, Dicembre 2017. www.trapiantipiemonte.it






