L’antigene core-relato del virus dell’epatite B (Hepatitis B core-related antigen; HBcrAg) è un marcatore composito di tre diverse proteine virali, tradotte dalla regione precore/core del virus dell’epatite B (HBV), ovvero l’antigene solubile “e” (HBeAg), l’antigene “core” (HBcAg), componente strutturale del nucleocapside virale, e una proteina core-relata da 22 kDa (p22cr), costituente il nucleocapside delle particelle di Dane difettive (empty particles) (1). Negli ultimi anni, la misurazione dei livelli circolanti di HBcrAg sta progressivamente diventando parte integrante della normale pratica clinica per la gestione dei pazienti con infezione cronica da HBV. I risultati di uno studio multicentrico europeo hanno mostrato che una singola misurazione di HBcrAg è utile nella diagnosi differenziale fra epatite cronica HBeAg-negativa e infezione cronica HBeAg-negativa; più del 90% dei soggetti portatori inattivi di HBV, che pertanto non necessitavano di trattamento antivirale, avevano valori di HBcrAg < 3,0 Log U/mL (2). Inoltre, l’HBcrAg risulta ad oggi il miglior surrogato della quantità e dell’attività replicativa di HBV covalently-closed-circular DNA (cccDNA) intraepatico, il minicromosoma che funge da stampo per i trascritti virali da cui derivano le proteine e il genoma maturo del virus (3,4); ne deriva che il marcatore sia particolarmente utile nel monitoraggio dei pazienti con epatite cronica in trattamento a tempo indefinito con analoghi nucleos(t)idici (Nuc) per monitorare l’attività replicativa intraepatica di HBV (5), e per identificare quei pazienti che potrebbero beneficiare di una interruzione del trattamento (6).
Recenti evidenze suggeriscono un significato clinico di HBcrAg anche nei pazienti con infezione cronica da virus dell’epatite D (HDV).
Quantificazione di HBcrAg in pazienti con epatite cronica D
Solitamente, HDV esercita un ruolo dominante su HBV, come testimoniato dai bassi livelli circolanti di HBV DNA e di HBV cccDNA nel fegato riscontrabili nei pazienti coinfetti HBV/HDV rispetto a quelli degli individui monoinfetti HBV. Tuttavia, già nei primi anni ’90, divenne evidente come la prognosi dei pazienti con infezione cronica D fosse influenzata dall’attività replicativa di HBV; nonostante l’assenza di sofisticate tecniche di biologia molecolare, si osservò che l’attiva replicazione di HBV era in grado di incrementare il potenziale patogenetico di HDV, determinando un danno epatico più severo e una maggiore incidenza di complicanze della cirrosi epatica, tra cui scompenso ascitico e carcinoma epatocellulare (hepatocellular carcinoma; HCC) (7). Oggi, la disponibilità di metodiche altamente sensibili per la quantificazione degli acidi nucleici e di nuovi test sierologici quantitativi ha permesso di delucidare specifici pattern associati all’attività e allo stadio della malattia di fegato in pazienti con epatite cronica D, confermando il ruolo dell’attività trascrizionale di HBV nel determinare la patogenicità di HDV.
In una coorte di 122 pazienti con coinfezione HBV/HDV provenienti da regioni europee a media ed elevata endemia per diffusione del virus (Italia e Romania, rispettivamente), è stata osservata una significativa correlazione fra i livelli circolanti di HDV RNA e HBcrAg (rs = 0.332; p < 0.001), a loro volta associati a incremento delle alanina-aminotransferasi (ALT) (OR = 2.37, 95%CI 1.46 – 3.84; p = 0.001) (8). Questi dati sono coerenti con la sostenuta attività trascrizionale di antigeni virali (antigene di superficie di HBV, HBsAg; antigene core di HBV; HBcAg) che si osserva nei pazienti con coinfezione HBV/HDV rispetto ai pazienti monoinfetti HBV, a fronte di una ridotta quantità intraepatica di HBV cccDNA e HBV RNA pregenomico (precursore dell’HBV DNA) (9).
Complessivamente, questi risultati suggeriscono che una più attiva trascrizione di HBV cccDNA sia necessaria a supportare la patogenicità di HDV; pertanto, la misurazione di HBcrAg si configura come un promettente strumento prognostico per la valutazione dei pazienti con epatite cronica D, e potrebbe rivelarsi utile per la stratificazione del rischio di insorgenza di eventi epatici nel medio-lungo termine.
HBcrAg nel trattamento dei pazienti con epatite cronica D
La terapia dell'epatite cronica D si basa principalmente sull’impiego di interferone alfa (IFNα), introdotto nella pratica clinica 30 anni fa. Tuttavia, i risultati sono modesti; solo un quarto dei pazienti trattati con IFNα ottiene una risposta virologica (HDV RNA-negativo a 24 settimane post terapia) a fronte di un’alta incidenza di effetti collaterali. Pertanto, la disponibilità di biomarcatori in grado di predire la risposta alla terapia e identificare i pazienti che hanno una ragionevole probabilità di beneficiare di trattamento antivirale rappresenta oggi un’urgente necessità medica.
Diversi studi hanno evidenziato l’utilità clinica di HBcrAg nel predire la risposta a terapia con IFNα pegilato (peg-IFNα) nei pazienti con epatite cronica B, sia HBeAg-negativa sia HBeAg-positiva. Recentemente, è stato evidenziato un potenziale ruolo di HBcrAg come predittore di risposta a terapia con peg-IFNα in associazione a tenofovir dipivoxil fumarato per 96 settimane in pazienti con epatite D (10). Sia al basale che in corso di terapia, livelli più bassi di HBcrAg presentavano un elevato valore predittivo negativo (NPV) per la negativizzazione di HDV RNA alla 24a settimana di follow-up post terapia, suggerendo che la misurazione di HBcrAg possa rappresentare un valido ausilio diagnostico sia per un’appropriata selezione dei pazienti che potrebbero beneficiare di trattamento antivirale sia per l’identificazione dei pazienti per i quali non è raccomandabile proseguire il trattamento per la bassa probabilità di ottenere una risposta. Questi risultati sono coerenti con quelli di un precedente studio pilota su 13 pazienti con epatite D, nel quale era stato osservato che la misurazione dei valori basali di HBcrAg e il loro declino alla 24a settimana in corso di trattamento con peg-IFNα in monoterapia consentiva di identificare con elevata accuratezza diagnostica i pazienti che avrebbero ottenuto una risposta virologica alla terapia con HDV RNA persistentemente negativo alla 48a settimana di follow-up (Figura 1) (11).
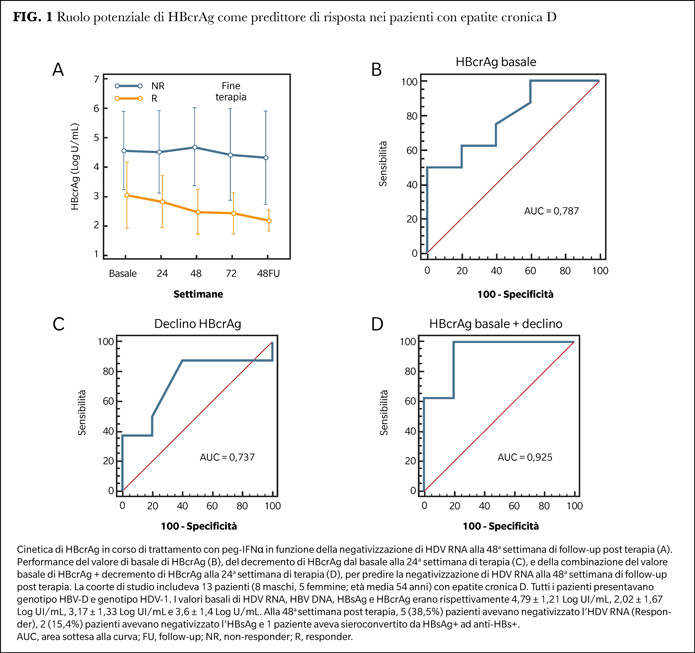
La rilevanza di HBcrAg nel trattamento dei pazienti con epatite D potrebbe dunque dipendere dall’effetto regolatorio dell’IFN sulla modulazione epigenetica di HBV cccDNA (12). La ridotta attività trascrizionale di HBV cccDNA si traduce in una diminuita espressione circolante di HBcrAg; il marcatore rappresenterebbe pertanto un fattore prognostico favorevole, non solo in termini di patogenicità di HDV, ma anche in termini di risposta a trattamento antivirale. A supporto di quest’ipotesi concorrono i risultati di diversi studi indipendenti condotti su pazienti con epatite cronica B, nei quali una ridotta quantità e attività trascrizionale di HBV cccDNA intraepatico, a cui si accompagnano bassi valori circolanti di HBcrAg e HBsAg, deporrebbe per un ridotto rischio di riattivazione virale in seguito a cessazione di terapia con Nuc (13).
Conclusioni
Ad oggi, pochi studi hanno investigato il potenziale ruolo clinico della misurazione di HBcrAg in pazienti con epatite cronica D. Tuttavia, i dati disponibili sono incoraggianti; studi futuri dovranno confermare il significato prognostico di HBcrAg nella progressione della malattia di fegato, nell’insorgenza di eventi clinici, e nella gestione dei pazienti con epatite cronica D in trattamento con IFN e nuovi farmaci in avanzata sperimentazione clinica.
- Mak LY, Seto WK, Fung J, et al. New Biomarkers of Chronic Hepatitis B. Gut Liver 2019; 13:589-595.
- Brunetto MR, Carey I, Maasoumy B, et al. Incremental value of HBcrAg to classify 1582 HBeAg-negative individuals in chronic infection without liver disease or hepatitis. Aliment Pharmacol Ther 2021; 53: 733-744.
- Testoni B, Lebossé F, Scholtes C, et al. Serum hepatitis B core-related antigen (HBcrAg) correlates with covalently closed circular DNA transcriptional activity in chronic hepatitis B patients. J Hepatol 2019; 70: 615-625.
- Caviglia GP, Armandi A, Rosso C, et al. Hepatitis B Core-Related Antigen as Surrogate Biomarker of Intrahepatic Hepatitis B Virus Covalently-Closed-Circular DNA in Patients with Chronic Hepatitis B: A Meta-Analysis. Diagnostics 2021; 11: 187.
- Caviglia GP, Abate ML, Noviello D, et al. Hepatitis B core-related antigen kinetics in chronic hepatitis B virus genotype D-infected patients treated with nucleos(t)ide analogues or pegylated-interferon-α. Hepatol Res 2017; 47: 747-754.
- Papatheodoridi M, Hadziyannis E, Berby F, et al. Predictors of hepatitis B surface antigen loss, relapse and retreatment after discontinuation of effective oral antiviral therapy in noncirrhotic HBeAg-negative chronic hepatitis B. J Viral Hepat 2020; 27: 118-126.
- Smedile A, Rosina F, Saracco G, et al. Hepatitis B virus replication modulates pathogenesis of hepatitis D virus in chronic hepatitis D. Hepatology 1991; 13: 413-416.
- Ricco G, Popa DC, Cavallone D, et al. Quantification of serum markers of hepatitis B (HBV) and Delta virus (HDV) infections in patients with chronic HDV infection. J Viral Hepat 2018; 25: 911-919.
- Pollicino T, Raffa G, Santantonio T, et al. Replicative and transcriptional activities of hepatitis B virus in patients coinfected with hepatitis B and hepatitis delta viruses. J Virol 2011; 85: 432-439.
- Sandmann L, Yurdaydin C, Deterding K, et al. HBcrAg Levels Are Associated With Virological Response to Treatment With Interferon in Patients With Hepatitis Delta. Hepatol Commun 2022; 6: 480-495.
- Olivero A, Caviglia GP, Ciancio A, et al. Basal values and on treatment decline of hepatitis B core-related antigen are predictive of response to interferon therapy in chronic hepatitis D. J Hepatol 2018; 68: S476.
- Lucifora J, Xia Y, Reisinger F, et al. Specific and nonhepatotoxic degradation of nuclear hepatitis B virus cccDNA. Science 2014; 343: 1221-1228.
- Sonneveld MJ, Park JY, Kaewdech A, et al. Prediction of Sustained Response After Nucleo(s)tide Analogue Cessation Using HBsAg and HBcrAg Levels: A Multicenter Study (CREATE). Clin Gastroenterol Hepatol 2022; 20: e784-e793.






